الذرة
الذرة هي أصغر وحدة هيكلية لعنصر كيميائي يحمل خصائصه المميزة. إنه أصغر جزء يمكن أن تنقسم إليه المادة ما دون إطلاق جزيئات مشحونة كهربائيًا. وبالتالي فهي وحدة البناء الأساسية للمادة والكيمياء أيضًا. أصل كلمة atom (بالإنجليزية: Atom) يرجع إلى atomus اللاتينية ، وهو ما يعني أنه غير قابل للتجزئة ، لأنه في ذلك الوقت كان يعتقد أنه لا يوجد شيء أصغر من الذرة ، وأنه لا يمكن تقسيم الذرة. [1] [2]
مكونات الذرة
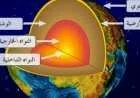
على عكس المعتقدات السابقة ، تتكون الذرة من أجزاء أصغر ، وهي: [2]
- النواة (باللغة الإنجليزية: النواة): النواة هي الجزء المركزي من الذرة ، التي تشكل معظم كتلتها ، اكتشف الفيزيائي إرنست رذرفورد (إرنست رذرفورد) ووجود النواة في عام 1911 ، وتشكل نواة البروتونات ، النيوترونات ، وتماسك المكونات الأساسية بفضل قوى الترابط النووي (باللغة الإنجليزية: قوة قوية).
- البروتونات : اكتشف راذرفورد وجود جزيئات مشحونة بشحنة موجبة داخل النواة ، تسمى البروتونات ، والتي تتكون بدورها من ثلاث جسيمات أولية تسمى الكواركات ، ويتم ترتيب الكواركات التي تتكون منها البروتونات في الأعلى والثانية في أسفل ، والبروتون لديه كتلة صغيرة تساوي 1.673 x10 -27 كجم.
- النيوترونات : النيوترونات (المحايدة) الموجودة داخل النواة ، افترض رذرفورد وجودها في عام 1920 م ، واكتشف العالم تشادويك في عام 1932 م ، وكانت كتلة النيوترونات أكبر قليلاً من كتلة البروتونات وتساوي 1.6749 × 10 - 27 ، والتي تتكون أيضًا من ثلاثة كواركات ، ولكن بترتيب مختلف ، واحد في الأعلى واثنان في الأسفل.
- الإلكترونات (باللغة الإنجليزية: الإلكترونات): قاموا بشحن الجسيمات سالبة الشحنة وجذبوا البروتونات المشحونة بالكهرباء ، واكتشفوا وجود العالم البريطاني جوزيف جون طومسون (JJ Thomson) في عام 1897 ، وهو عبارة عن لف من الإلكترونات وفقًا للنموذج الذي طوره العالم إروين شرودنجر في مدارات محددة حول النواة ، أصغر من البروتونات والنيوترونات وأكثر من 1800 مرة ؛ تساوي كتلته 9.109x10 -31. من خلال دراسة ترتيب الإلكترونات حول النواة ، يمكن التنبؤ ببعض الخصائص الفيزيائية للذرة ، مثل الثبات ونقطة الغليان والتوصيل.
تاريخ الذرة
في عام 440 قبل الميلاد ، افترض الفيلسوف Democritus أن المواد تتكون من جزيئات صغيرة لا يمكن تجزئتها وتسمى الذرات ، وأن الكون يحتوي على عدد لا حصر له من الذرات التي تتحرك باستمرار ، وأن الذرات تتجمع لتشكل المادة ، لكنها لا تندمج لتكوين ذرات جديدة ، قدم Democritus نظريته الذرية للعالم في ذلك الوقت ، ولكن رفضها فلاسفة آخرون ، بقيادة أرسطو الذي اعتقد أن كل شيء تم إنشاؤه من الأرض والنار ، والهواء وفي عام 1803 م ، الكيميائي البريطاني جون دالتون نظريته الذرية ، التي صاغها بعد دراسة الفكر Democritus ، وتنص نظريته على أن ذرات عنصر واحد هي نفسها ، وأن ذرات العناصر المختلفة تختلف عن بعضها البعض في الوزن والخصائص ، وأن الذرات لا يمكن يتم إنشاؤه أو تدميره ، وهذه المسألة تتكون من اتحاد الذرات مع بعضها البعض. [2]
في عام 1897 م ، أثبت العالم تومسون ، مكتشف الإلكترون ، أنه يمكن تقسيم الذرة. في نفس العام ، قدم طومسون نموذج فطيرة الزبيب (بالإنجليزية: Plum Pudding Model) ، والذي يمثل الذرة ككرة موجبة الشحنة يتم فيها توزيع جسيمات سالبة الشحنة (الإلكترونات). فطيرة ، لذلك يتم شحن الذرة بالتساوي. في عام 1911 م ، نشر العالم رذرفورد نظريته الذرية ، التي تنص على أن الذرة تتكون من نواة صغيرة موجبة الشحنة ، تدور حولها الإلكترونات ، وأن معظم مساحة الذرة فارغة. بعد ذلك ، أوضح العالم نيلز بور خصائص الإلكترونات ، وبعدها جاء العالم ايرفين ايروين شرودنجر الذي طور النموذج الكمومي للذرة ، والعالم فيرنر هايزنبرغ الذي ذكر أنه لا يمكن معرفة موقع الإلكترون وسرعته في الوقت نفسه الوقت ، وبعد ذلك اكتشف العالمان (بشكل منفصل) موراي جيل مان وجورج زويج (جورج زويغ) أن كلا البروتونات والنيوترونات مصنوعان من الكواركات في. [2]
خصائص الذرة
للذرات خصائص عديدة ، منها:
- الرقم الذري للعنصر هو عدد البروتونات في نواة الذرة ، والتي تحدد الخصائص الكيميائية للعنصر. [3]
- الذرة المحايدة هي الذرة التي يكون عدد البروتونات فيها مساوياً لعدد الإلكترونات. [3]
- الكتلة الذرية لعنصر ما هي مجموع عدد البروتونات والنيوترونات في النواة ، المقاسة بوحدات (الكتلة الذرية) ، ووحدة الكتلة الذرية تساوي 1/2 كتلة ذرة الكربون. [3]
- تكون الكتلة الذرية أقل من كتلة الذرة ، لأن كتلة الذرة تتكون من كتلة النواة بالإضافة إلى كتلة الإلكترونات ، وهي كتلة صغيرة مقارنة بكتلة البروتونات والنيوترونات. [3]
- يحتوي كل عنصر كيميائي على العديد من النظائر (بالإنجليزية: Isotopes) ، والتي هي أشكال للعنصر الكيميائي لذريتها بنفس العدد الذري (عدد البروتونات) ، ولكنها تختلف في الكتلة الذرية بسبب اختلاف عدد النيوترونات ، لا تختلف الخصائص الكيميائية للعنصر ونظيره. [3]
- تحافظ الإلكترونات على مسارها في مدارات حول النواة بفضل قوى الجاذبية التي تنشأ بين البروتونات الموجبة الشحنة والإلكترونات سالبة الشحنة. [3]
- يدور الإلكترون حول النواة ، وفي الوقت نفسه يدور حول نفسه ، وتسمى هذه الظاهرة باللف المغزل أو الدوران (بالإنجليزية: Spin) ، وهذا يولد لحظة مغناطيسية تبلغ 9.28 × 10 -24 -. [3]
- توجد الإلكترونات في مستويات متتالية تسمى مستويات الطاقة ، ويمتد كل مستوى إلى عدد محدد من الإلكترونات ، ويمتد المستوى الأول إلى إلكترونين ، بينما يمتد الثاني إلى ثمانية إلكترونات. [4]
- تصل الذرات إلى الاستقرار ، إما عن طريق فقدان أو الحصول على الإلكترونات ، أو عن طريق مشاركتها. [4]
- تحتوي الذرات الموجودة في مدارها الأخير على إلكترون أو إلكترونين أو ثلاثة إلكترونات تخسرها عند تفاعلها مع ذرات في مدارها الأخير والتي تحتوي على خمسة أو ستة أو سبعة إلكترونات. [4]
- تميل الذرات التي تحتوي على خمسة أو ستة أو سبعة إلكترونات في مدارها الأخير إلى اكتساب الإلكترونات عندما تتفاعل مع الذرات في مدارها الأخير والتي تحتوي على إلكترون أو اثنين أو ثلاثة إلكترونات. [4]
- لا تميل الذرات التي تحتوي على أربعة إلكترونات في مدارها الأخير إلى فقدان أو الحصول على الإلكترونات. [4]
المراجع
- ↑ "atom" , www.dictionary.com , Retrieved 26-9-2017. Edited.
- ^ أ ب ت ث Tim Sharp (8-8-2017), "What is an Atom" ، /www.livescience.com , Retrieved 26-9-2017. Edited.
- ^ أ ب ت ث ج ح خ "Atom" , www.britannica.com , Retrieved 26-9-2017. Edited.
- ^ أ ب ت ث ج " ChemistryInorganic ChemistryStructure of an Atom Top Structure of an Atom " , chemistry.tutorvista.com , Retrieved 26-9-2017. Edited.